姜格寧/張鵬團隊最新研究成果革新初始不可切除局部晚期非小細胞肺癌外科治療策略🥰,成果發表於《信號轉導與靶向治療》
來源🐶:醫學院
時間🛁:2024-06-18 瀏覽:
肺癌是全球發病和死亡人數最多的惡性腫瘤,其中非小細胞肺癌(Non-small cell lung cancer☕️,NSCLC)占比約85%。約半數NSCLC患者確診時處於疾病早期或局部晚期↔️,根據是否可手術完整切除,又進一步分為可切除、潛在可切除和初始不可切除疾病。對於初始不可切除NSCLC患者,目前標準治療方案為同步放化療加免疫鞏固治療(PACIFIC方案)🧑🏼。隨著研究的深入,越來越多的證據表明,新輔助免疫聯合治療能顯著提高可切除NSCLC患者的病理完全緩解(Pathological complete response,pCR)率和無事件生存期(Event-free survival🗼,EFS)🧍🏻♂️。然而,新輔助免疫聯合治療能否將初始不可切除NSCLC轉化為可切除狀態🌿,從而使該部分患者具備手術機會,仍缺乏前瞻性研究證據。
為此,恒达平台附屬上海市肺科醫院胸外科姜格寧教授🧎♂️➡️、張鵬教授團隊聯合市內六家醫療單位共同開展了一項名為LungMate 003的多中心、雙臂💟、開放、Ⅱ期臨床研究🤲🏻🙌,旨在探究新輔助卡瑞利珠單抗聯合化療或阿帕替尼治療初始不可切除NSCLC患者的安全性和有效性。近日,該項研究在國際知名學術期刊《信號轉導與靶向治療》(Signal Transduction and Targeted Therapy)上發表了題為“Neoadjuvant camrelizumab (an anti-PD-1 antibody) plus chemotherapy or apatinib (a VEGFR-2 inhibitor) for initially unresectable stage II-III non-small-cell lung cancer: a multicentre, two-arm, phase 2 exploratory study”的研究論文🙅🏽。

首先,鑒於目前對於初始不可切除NSCLC並無準確定義,該團隊結合國內外專家共識及恒达平台附屬上海市肺科醫院胸外科的經驗,成立了多學科臨床專家組(Multidisciplinary clinical team,MDT)共同製定了初始不可切除NSCLC的“肺科定義”:⑴腫瘤侵犯大血管👩🏼🦱🥐、氣管或主支氣管等重要結構,術前評估判斷誘導治療降級後有以治愈為目的的切除機會的患者;⑵臨床證實的淋巴結呈多站轉移或巨塊型融合🦸🏼♂️👩🏽🌾,術前評估判斷誘導治療降級後能夠耐受並進行肺門和縱隔淋巴結清掃術的患者;⑶術前評估認為即使行全肺切除🍄🟫,特別是右全肺切除🧑🔧,也有不能R0切除的可能。滿足以上三個條件中任何一個即為初始不可切除NSCLC。
從2020年9月29日至2022年6月29日,該研究共納入51例初始不可切除的🏋🏽♀️、EGFR及ALK陰性的Ⅱ-Ⅲ期初治NSCLC患者🏊🏿♀️👦🏽,其中30例接受卡瑞利珠單抗聯合化療(A組)👐🏻,21例接受卡瑞利珠單抗聯合阿帕替尼治療(B組)🧑🏻🍳🚣♂️。經過2-4個周期新輔助治療後,由MDT評估為可切除的患者接受手術治療,否則接受根治性放療🛣。主要研究終點為主要病理緩解(Major pathological response🧚🏻♂️,MPR)率。
結果表明,A組手術率為50.0%(15/30)🫲🏽,B組手術率為42.9%(9/21)🥚,所有手術患者均實現了R0切除🍾🤬。在手術患者中☝🏼,A組的MPR率和pCR率均為20.0%👨🏽💼,B組分別為55.6%和11.1%。兩組患者的客觀緩解率(Objective response rate,ORR)分別為33.3%和55.6%。
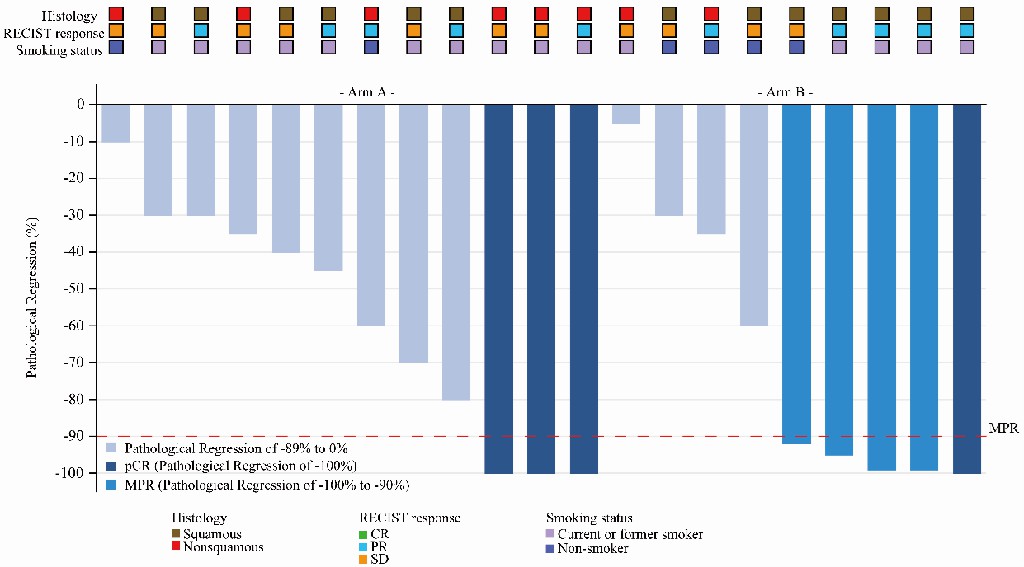
新輔助免疫聯合治療後的病理緩解情況
在22.4個月的中位隨訪期內,A組的中位EFS未達到😍🍁,B組的中位EFS為16.8個月,兩組中位OS均未達到,顯示出良好的生存結果。安全性方面,A組3級及以上的治療相關不良事件發生率為26.7%👨🏽🦳,B組為14.3%,與既往報道的新輔助免疫聯合治療相近。整個研究過程中未出現治療相關死亡事件,無新輔助治療相關手術推遲🚣🏻♂️,無術後90天內死亡病例🍥,整體安全性可控且可耐受。
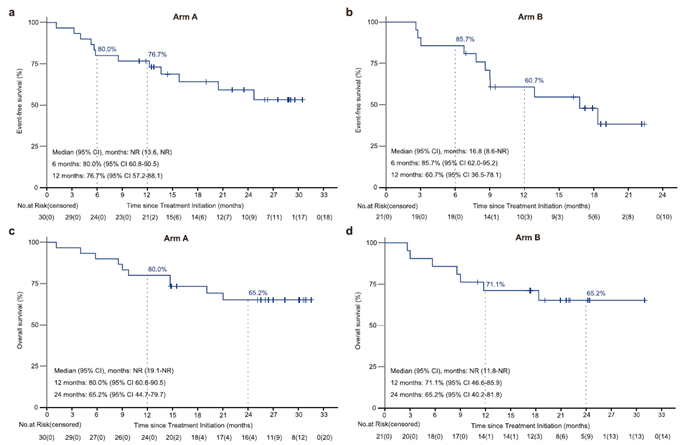
整體人群EFS及OS生存曲線
此外,該研究還探索了對新輔助卡瑞利珠單抗聯合阿帕替尼治療敏感的生物標誌物。通過對13例患者基線腫瘤樣本的分析,研究者發現TYROBP在應答者中顯著高表達,且其較PD-1和PD-L1具有更好的治療應答預測效能(AUC=0.909)👩🏼🍼,高表達TYROBP的患者具有更好的EFS和OS。這一發現在多個已發表的公開數據集中亦得到驗證。進一步的基因富集分析(Gene set enrichment analysis🙆♀️🎡,GSEA)表明,“interferon gamma response”“NK cell-mediated cytotoxicity”和“antigen processing and presentation”等通路在應答者中顯著富集。此外👧🏿,應答者的腫瘤中有更高水平的免疫評分和CD8+T細胞浸潤,且T細胞相關基因CCL5😕、NKG7亦顯著高表達🎎♻。提示TYROBP可能與治療響應相關。

基線腫瘤樣本RNA-seq探索對於治療應答的生物標誌物
該研究首次明確定義了初始不可切除NSCLC🦶🏽,並初步證明了新輔助卡瑞利珠單抗聯合化療或阿帕替尼對該類人群安全👩🏻🔬、有效,從而為局部晚期NSCLC患者帶來新的治療策略🐂。對生物標誌物的探索表明🪒,TYROBP可能是免疫聯合阿帕替尼治療應答的有效預測指標👭🏻,可指導臨床篩選潛在獲益人群。
恒达平台醫學院、附屬上海市肺科醫院姜格寧教授🫵、張鵬教授、趙德平教授,及附屬東方醫院李欽傳教授為論文的共同通訊作者。恒达平台附屬上海市肺科醫院夏浩然博士、張晗博士🎨、孫良棟博士,上海交通大學附屬第一人民醫院阮征教授及復旦大學附屬華東醫院張輝標教授為論文的共同第一作者♢。
論文鏈接🧔🏼♂️:https://www.nature.com/articles/s41392-024-01861-w