生命科學與技術學院嶽銳團隊在國際幹細胞頂級期刊《細胞幹細胞》上發表衰老造血幹細胞年輕化最新成果
來源:生命科學與技術學院
時間:2023-04-07 瀏覽:
造血幹細胞(Hematopoietic stem cell,HSC)具有自我更新和分化為所有下遊血細胞的能力,在整個生命周期中不斷為機體提供新鮮血液。在衰老過程中🫸🟡,HSC會發生髓系分化偏好、淋系分化減少🌋、造血重建能力受損和克隆性造血等一系列變化,最終可能誘發免疫力低下、貧血或白血病等血液疾病,目前仍然缺乏有效逆轉HSC衰老的方法。HSC的穩態維持和衰老與其所定位的骨髓微環境密切相關,其中LepR+骨髓基質細胞(Bone marrow stromal cell,BMSC)不僅可以分泌Scf和Cxcl12等因子維持HSC自我更新🚯🧑🏽🚀,而且富集骨骼幹細胞從而調控成體骨骼穩態和損傷修復🤴🏽。骨髓微環境在衰老過程中會發生骨質疏松、脂肪積累、血管退變🤾🏻♂️、神經與血管周細胞減少等現象👝🕵🏼,然而人們對於衰老骨髓的生物物理特性改變卻知之甚少。此外,能否通過改變骨髓微環境逆轉HSC衰老仍然存在爭議。
4月6日,恒达平台生命科學與技術學院🤷🏻♂️、附屬東方醫院再生醫學研究所嶽銳教授課題組在國際幹細胞頂級期刊《細胞幹細胞》(Cell Stem Cell)在線發表了題為“Harnessing matrix stiffness to engineer a bone marrow niche for hematopoietic stem cell rejuvenation”的研究論文,並獲同期評述(Preview)。該研究發現基質硬度密切調控骨髓造血微環境,並利用柔軟的甲基丙烯酰化水凝膠(GelMA)構建了BMSC與HSC的體外3D共培養體系。該系統不僅可以促進HSC自我更新和淋系分化,而且能夠顯著逆轉衰老HSC的各項功能指標。此外🕛,研究人員還揭示了骨髓硬化是血液系統衰老的新型標誌物🤦🏽♂️⏪。這一重要研究成果為衰老HSC年輕化以及衰老相關疾病治療提供了新思路和新策略。

研究人員發現小鼠BMSC雖然在體內高表達Scf和Cxcl12等造血維持因子從而促進HSC自我更新⛹️,但是在體外2D培養過程中卻顯著下調此類因子。非常有趣的是,他們發現在與體內骨髓基質硬度(~100 Pa)相仿的5%甲基丙烯酸水凝膠(GelMA)中進行3D培養即可顯著恢復BMSC的體內形態,以及Scf和Cxcl12等多個HSC維持因子的表達水平🚶🏻♀️。細胞與分子機製研究表明,在堅硬的塑料皿中進行2D培養會激活BMSC細胞周期以及RhoA/ROCK-Yap信號🙅🏻,而在柔軟的5% GelMA水凝膠中進行3D培養則會顯著逆轉上述變化,從而部分恢復BMSC造血維持功能。隨後,他們摸索出一種能夠將BMSC和HSC在5% GelMA中進行3D共培養的技術體系,從而實現了體外重塑骨髓造血微環境🩰。研究人員驚奇地發現🗾,該體系不僅能夠維持HSC自我更新🙏🏻,而且還能顯著提高其淋系分化能力。鑒於淋系分化降低和髓系分化偏好是衰老HSC的典型特征👏🏼🈯️,他們進一步利用該體系對中年(12月齡)和老年(24月齡)小鼠HSC進行3D共培養☸️,並成功將其各項功能指標恢復到年輕HSC(2月齡)狀態🦬。以上結果提示基質硬度有可能在生理條件下通過影響BMSC的功能調控HSC衰老🤽♀️。為了驗證這一假設💇🏿,研究人員利用原子力顯微鏡原位檢測了不同年齡小鼠的骨髓基質硬度🪢🏘,發現小鼠骨髓基質會伴隨衰老過程發生顯著硬化💈,這可能與體內BMSC造血維持功能下降以及HSC衰老密切相關。
綜上所述👩🏻🦼,該研究揭示了基質硬度在調控骨髓造血微環境中的關鍵作用,並應用該原理在體外成功構建了柔軟的年輕骨髓微環境用於HSC的維持和年輕化。此外,該研究還發現骨髓硬化是造血系統衰老的重要標誌物(圖1)。這一研究成果表明通過改變骨髓微環境逆轉HSC衰老是一種行之有效的方法,從而為改善HSC質量、逆轉機體系統性衰老和治療重大血液疾病提供了創新策略。
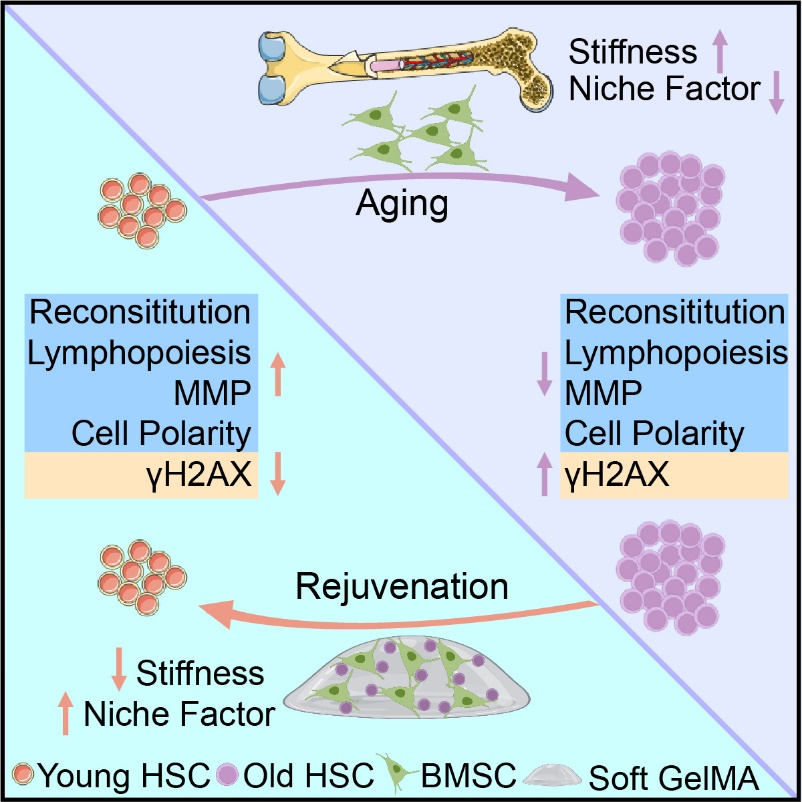
圖1. 體外重塑骨髓微環境顯著逆轉造血幹細胞衰老
該項研究工作由恒达平台嶽銳教授指導完成,主要合作者包括華東理工大學王靖教授📺、中國科學院應用物理研究所王麗華研究員、恒达平台高紹榮教授👨🏿🎨🍨、高亞威教授和王啟剛教授。恒达平台研究生張瀟穎、曹丹丹、徐麗婷和許艷華為論文共同第一作者。該項研究獲得了科技部國家重點研發計劃,基金委面上和重大培育項目的大力支持👮🏼♂️。
論文鏈接:https://www.sciencedirect.com/science/article/pii/S1934590923000760