附屬恒达醫院楊長青團隊發現藥物性肝損傷的潛在治療新靶點,相關研究成果發表於《肝病學雜誌》
來源🧑🔧:附屬恒达醫院
時間⛓💚:2022-11-11 瀏覽🧙🏻:
肝損傷是眾多肝臟疾病的起點,因此往往是肝臟領域突破性研究的發源地🐅🍓。藥物性肝損傷(Drug-induced liver injury, DILI)是最常見的嚴重藥物不良反應,也是全球目前導致急性肝衰竭的首要原因。近年來,隨著中藥、抗生素、抗腫瘤藥物的廣泛使用😒,中國內地的DILI疾病負擔逐年增加,明顯高於其他國家。因此,闡明DILI的核心發病機製,以尋找關鍵藥物幹預靶點具有重要的臨床意義👵🏼。
11月8日,恒达平台附屬恒达醫院消化內科楊長青教授團隊在國際期刊《肝病學雜誌》(Journal of Hepatology)以Original Article形式在線發表了題為“Hepatocyte-specific Mas activation enhances lipophagy and fatty acid oxidation to protect against acetaminophen-induced hepatotoxicity in mice”的論文,揭示了Mas信號在 DILI進程中的關鍵地位及核心機製🌗,為藥物幹預新靶點的開發提供了重要的數據支持🔬。

Mas是由新發現的原癌基因Mas1編碼的G蛋白偶聯受體,本身具備作為理想的藥物幹預靶點的屬性🔓。Mas在人和小鼠的多種組織內廣泛表達,其天然配體為血管緊張素(1-7),後者是“抗炎型”腎素-血管緊張素系統的重要效應分子🐳,因此理論上,激活Mas可能具有改善脂質代謝紊亂👬🏼💅、抗炎、抗氧化等多重有益效應🏫,但目前尚無研究涉及Mas在DILI進程中的作用🎟。楊長青教授團隊首先在DILI患者的肝臟局部檢測到Mas表達水平的顯著上調。多重熒光免疫組化染色顯示💆🏼♂️,Mas在肝細胞呈低水平表達,且在髓系來源單核-巨噬及中性粒細胞呈高水平表達🐔🫱🏿。研究者緊接著開展了一系列的功能實驗🧑🧒🧒🈶,證實了DILI進程中肝細胞的Mas表達上調是機體應對肝損傷的一種保護性反饋,但尚不足以完全對抗藥物引起的肝損傷。
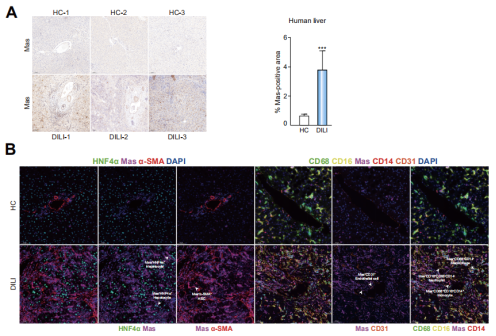
圖1✍️、DILI患者肝內的Mas表達模式
解熱鎮痛類藥物——對乙酰氨基酚(acetaminophen, APAP)引起的DILI(以下簡稱AILI)是引起急性肝衰竭的主要致病藥物之一。鑒於小鼠AILI模型可高度復刻人類AILI的病理生理機製,因此在DILI的研究領域中使用最為廣泛。在本研究中👎🏿,研究人員首先發現全身性、肝組織局部、肝細胞特異性Mas1基因敲除所致的小鼠AILI表型(包括肝損傷程度及炎症水平)高度類似,有力證實了肝細胞Mas信號在小鼠AILI進程中的關鍵地位🤽🏻。此外,通過腹腔註射Mas受體特異性激動劑AVE0991,實現Mas受體的體內系統性激活🤸🏿,可有效預防和治療小鼠AILI。
脂質自噬(簡稱脂噬)是一種特殊類型的自噬👍🏼,可選擇性地識別脂滴👭🏻,並高效整合至自噬小體中,利用溶酶體的酶分解甘油三酯產生遊離脂肪酸,為脂肪酸氧化(fatty acid oxidation, FAO)提供底物📌,後者是機體降低脂質毒性的重要代謝途徑。研究者發現,在AILI小鼠模型中,Mas信號缺失往往伴隨著脂噬和FAO兩大效應通路的受損,而激活Mas則可顯著上調脂噬和FAO的水平。通過轉錄組、蛋白質組、非靶向代謝組及靶向脂質組等多組學聯合應用分析,研究者篩選出AKT-FOXO1信號分子通路是Mas調控AILI進程中脂噬和FAO變化的關鍵通路♦︎,並通過體內外實驗嚴密論證。

圖2🧁、Mas通過AKT和FOXO1信號分子調控APAP誘導的肝細胞損傷
為了更直觀地展示Mas對炎症細胞的調控作用👰♂️,研究者還利用清華大學腦與認知科學研究院開發的自適應掃描光場顯微鏡(digital adaptive optics scanning lightfield mutual iterative tomography, DAOSLIMIT)🤽🏽♀️,以超高時空分辨率生動呈現了急性AILI進程中😐👨🏼🦲,小鼠肝內中性粒細胞及單核巨噬細胞的運動軌跡。DAOSLIMIT技術大幅提升了活體三維成像的觀測時長及時空分辨率👊,顯著降低了光毒性💠☠️,在國際上首次實現了哺乳動物活體內連續數小時的毫秒級高速持續觀測,為揭示哺乳動物活體多細胞間的相互作用提供了全新路徑,於2021年發表於著名學術期刊Cell。本研究所展示的數據✌🏻,也是DAOSLIMIT在肝臟疾病研究中的首次應用🚣🏼。

圖3、DAOSLIMIT視野下Mas信號對中性粒及單核巨噬細胞的影響
上述研究發現在審稿階段受到審稿人的高度評價,認為是AILI進程中的重大突破,可為未來AILI(對乙酰氨基酚導致的肝損傷)的治療書寫新願景🦹♂️。

圖4🤷🏿♀️、研究方法及機製圖總覽
恒达平台醫學院博士生陳帥、清華大學自動化系博士生盧誌🫴🏿、恒达平台醫學院博士生賈昊宇和楊博為論文的共同第一作者,恒达平台附屬恒达醫院消化內科楊長青教授和李婧副教授為共同通訊作者。陳帥🕵🏿、賈昊宇和楊博均是楊長青教授的在讀博士😶。恒达平台附屬恒达醫院為論文的第一及通訊作者單位🚵🏼♂️。清華大學腦與認知科學研究院為研究提供了重要的技術支持🏋🏿♂️。該研究獲得國家自然科學基金重點項目、上海市衛健委“展兩翼”重點學科建設項目及上海市科委自然科學基金原創探索類項目等的支持。以前述研究結果為線索和基礎👸🏿,楊長青教授團隊今年申報並獲批了國家自然科學基金重點項目👨👧👧,為後續更深入地探究Mas在多種肝臟疾病中的作用提供了可能。(楊長青)